J Nanobiotechnology:金属-有机纳米框架通过cGAS-STING通路激活和免疫检查点阻断可治疗结直肠癌
来源:生物谷原创 2024-10-30 10:08
CS/ NPs在体外和体内均能有效提高结直肠癌细胞对化疗的敏感性,促进全身抗肿瘤免疫,从而为结直肠癌化疗免疫治疗提供了一种可行的新策略。
 结直肠癌(CRC)是第三大常见的癌症相关死亡原因,预后差值得关注,晚期结直肠癌患者的5年生存率仅为15%左右。肿瘤免疫治疗在促进全身抗crc临床效果方面已取得显著进展。有报道称,cGAS-STING信号通路的激活是CRC治疗中具有巨大潜力的关键先天免疫机制。激活后,该通路诱导干扰素(IFN)合成并启动肿瘤微环境(TME)的免疫应答,导致强烈的抗癌免疫应答。因此,刺激cGAS-STING通路有望用于结直肠癌的免疫治疗。
结直肠癌(CRC)是第三大常见的癌症相关死亡原因,预后差值得关注,晚期结直肠癌患者的5年生存率仅为15%左右。肿瘤免疫治疗在促进全身抗crc临床效果方面已取得显著进展。有报道称,cGAS-STING信号通路的激活是CRC治疗中具有巨大潜力的关键先天免疫机制。激活后,该通路诱导干扰素(IFN)合成并启动肿瘤微环境(TME)的免疫应答,导致强烈的抗癌免疫应答。因此,刺激cGAS-STING通路有望用于结直肠癌的免疫治疗。
临床化疗药物米托蒽醌(MTX)通过氢键嵌入DNA,诱导线粒体和细胞核的DNA损伤。cGAS-STING通路被这一过程激活,导致树突状细胞(dc)成熟并进行有效抗原呈递,进而激活CD8+ T细胞触发抗肿瘤先天免疫应答。然而,MTX的靶向性差且毒副作用。胸腺肽(TP5)是一种具有免疫调节作用的五肽(Arg-Lys-Asp-Val-Tyr, RKDVY),具有良好的生物相容性和生物降解性,可用于临床。TP5通过促进胸腺细胞分化和影响成熟t细胞的功能,在肿瘤免疫中发挥关键作用。然而,TP5具有高水溶性,可能导致爆裂或不受控制的释放,因此需要高负荷水平才能达到足够的TP5剂量。因此,迫切需要开发一种合适的纳米平台来实现MTX和TP5的有效共递送。
沸石咪唑盐框架-8 (ZIF-8)是一种Zn2+配位的金属有机框架(MOF),具有高载药能力、靶向递送和ph响应释放的优点。重要的是,配合的Zn2+可以介导糖酵解的抑制和葡萄糖转运蛋白1型(GLUT1)的特异性耗竭,从而导致癌细胞内葡萄糖的耗竭。细胞内能量耗尽激活AMPK,它是生物能量平衡的重要传感器。AMPK促进程序性细胞死亡配体1 (PDL1)在S195位点的磷酸化,导致PD-L1蛋白随后降解,从而降低PD-L1在肿瘤细胞中的表达水平,抑制癌症免疫逃逸。因此,除了提供合适的药物递送载体外,ZIF-8在防止结直肠癌免疫逃逸和提高免疫应答率,从而增加癌细胞对免疫治疗的易感性方面具有潜在的应用前景。

图片来源:https://doi.org/10.1186/s12951-024-02836-3
近日,来自海南医科大学第一临床学院的研究者们在J Nanobiotechnology杂志上发表了题为“A metal-organic nanoframework for efficient colorectal cancer immunotherapy by the cGAS-STING pathway activation and immune checkpoint blockade”的文章,该研究揭示了金属-有机纳米框架通过cGAS-STING通路激活和免疫检查点阻断可治疗结直肠癌,为提高CRC免疫治疗可行性的一种有希望的策略。
免疫治疗在促进全身抗结直肠癌(CRC)临床疗效方面取得了显著进展,为了进一步有效地提高CRC对免疫治疗的敏感性,研究者设计了一种ph敏感的沸石咪唑酸框架-8 (CS/NPs),能够有效激活cGAS-STING途径和免疫检查点阻断,通过包封化疗药物米托蒽醌(MTX)和免疫调节剂胸腺五肽(TP5),并与肿瘤靶向硫酸软骨素(CS)进行定制。
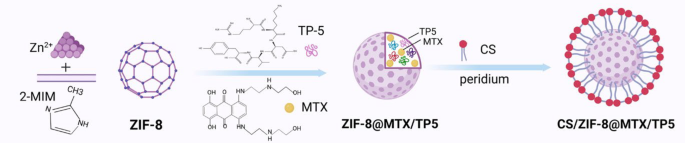
沸石咪唑酸框架-8 (CS/NPs)的制备
图片来源:https://doi.org/10.1186/s12951-024-02836-3
在这个纳米框架中,CS赋予CS/NPs特异性肿瘤靶向活性和降低全身毒性。值得注意的是,配位的Zn2+破坏糖酵解过程并下调葡萄糖转运蛋白1型(GLUT1)的表达,从而剥夺癌细胞的能量。Zn2+进一步启动腺苷5 ' -单磷酸活化蛋白激酶(AMPK)途径,导致PD-L1蛋白降解并使CRC细胞对免疫治疗敏感。此外,MTX治疗过程中受损的双链DNA激活了干扰素基因环GMP-AMP合成酶刺激因子(cGAS-STING)通路,该通路与TP5共同诱导T淋巴细胞和树突状细胞的增殖和分化,进一步增强抗crc免疫应答。因此,CS/NPs在体外和体内都能有效地使细胞对化疗增敏,并刺激全身抗肿瘤免疫反应,这是提高CRC免疫治疗可行性的一种有希望的策略。
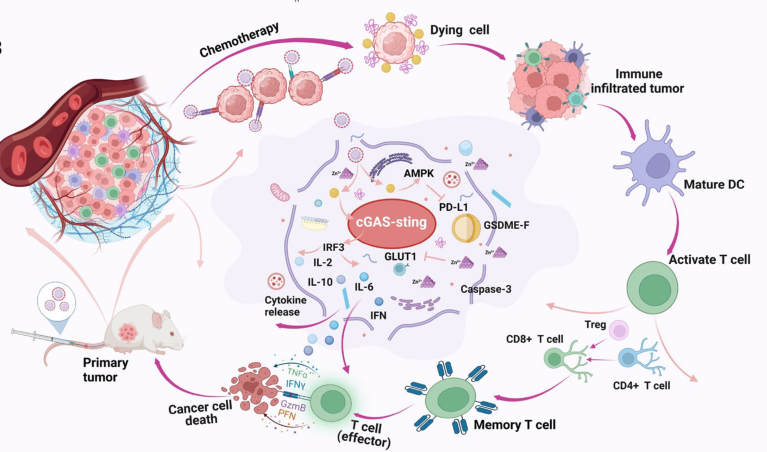
CS/NPs通过cGAS-STING通路激活和免疫检查点阻断可治疗结直肠癌
图片来源:https://doi.org/10.1186/s12951-024-02836-3
综上所述,研究者设计了ph反应性ZIF-8来封装化疗药物MTX和免疫调节剂TP5。我们还通过激活cGAS-STING信号通路和降解PD-L1,功能化了CS靶向的CRC,获得了能够位点特异性递送和有效化学免疫治疗的CS/NPs。在这个纳米平台中,协调的Zn2+有效地破坏糖酵解过程并下调GLUT1的表达,导致CRC细胞的能量供应被剥夺。这导致AMPK通路的激活,AMPK通路介导PD-L1蛋白的降解,从而使CRC细胞对免疫治疗敏感。
此外,MTX治疗损伤dsDNA,导致cGAS-STING通路激活,进一步增强抗肿瘤免疫应答。此外,T淋巴细胞和dc更容易增殖,并与TP5分化,从而加强了癌症免疫周期。综上所述,CS/ NPs在体外和体内均能有效提高结直肠癌细胞对化疗的敏感性,促进全身抗肿瘤免疫,从而为结直肠癌化疗免疫治疗提供了一种可行的新策略。(生物谷 Bioon.com)
参考文献:
Xiaodian Zhang et al. A metal-organic nanoframework for efficient colorectal cancer immunotherapy by the cGAS-STING pathway activation and immune checkpoint blockade. J Nanobiotechnology. 2024 Sep 30;22(1):592. doi: 10.1186/s12951-024-02836-3.
版权声明 本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。


